腹茧症(abdominal cocoon, AC)是一种临床罕见的腹膜病变,目前病因仍不明。长期以来,由于临床认识不够,术前漏诊、误诊较多。近年来,随着社会环境的变化和人们生活方式的改变,发病率有升高趋势,现将有关病因、临床特点、近年诊治进展等综述如下。
一、定义及命名
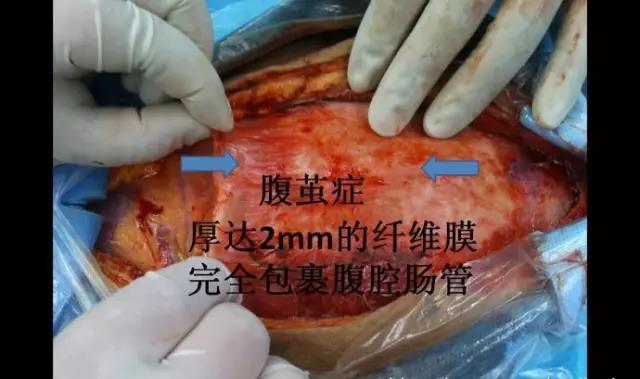
AC是一种临床罕见、病因不明、由纤维膜包裹部分或全部双调和肠造成完全性或不全性肠梗阻,以腹部包块为主要表现的腹部疾病,其特点是腹腔全部或部分脏器被一层致密灰白色形似蚕茧、质韧的纤维膜所包裹,形似蚕茧,故也称腹腔茧状包裹症,或先天性小肠禁锢症、局限性小肠外膜包绕症、小肠节段性纤维包裹症、包膜内粘连性肠梗阻等。1978年Foo等将其命名为“腹茧症”。
二、病因及发病机制
1、地理及环境因素:多发生于热带及亚热带地区,Seng等曾猜测与某种地区性病原体感染有关,Deeb等则认为高温所候可能致腹膜发育异常。在中国,57%的病例分布在沿海的华东地区,属亚热带季风气候,推断其发病与气候可能有一定关系。
2、性别及年龄因素:多见于青年女性及久婚不育者,男性发病少于女性,有文献统计我国患者最大发病年龄为79岁,最小2岁,男女比例为1:1.35。
3、腹膜先天性发育异常:文献曾报道4例儿童腹茧症病例,年龄6~8岁,既往均无手术、腹膜炎及长期服药史,认为该病与先天性胚胎发育异常有关。此外,术中见多数患者存在大网膜缺如或缩短,推测病变纤维膜可能由大网膜变异而来。
4、原发性腹膜炎(亚临床型非特异性腹膜炎性反应):女性生殖逆行感染、血源性或医源性腹腔感染,异物、结核、腹水等因素刺激腹膜引起纤维蛋白渗出,继而因成纤维细胞和毛细血管长入,机化形成纤维性包裹。Yip Francis和Lee推测本病可能是由某种地方性经生殖道侵入的病原体逆行感染引起的亚临床性腹膜炎的后遗症。Afthenporles等报道长期门诊腹膜透析患者的一个严重并发症即AC,随后研究表明向小鼠膜腔内注射酸性透析液可导致炎似人类AC的纤维包膜。Lallo等报道结核性腹膜炎也可造成AC。国内亦有腹部外伤、炎性反应致小肠茧状包裹有腹腔内化学治疗后AC的报道。
5、药物因素:Seng等认为β-受体阻滞剂(如盐酸普萘洛你片)可导致细胞过度增殖、胶原蛋白过量产生及腹腔纤维化,但国内外报道的绝大多数AC患者都没有长期服用此类药物史,显然这种推测尚缺乏足够的支持。
6、腹膜间皮细胞(PMC)的成骨性转化:有实验表明,PMC在体外培养可转化为成骨细胞素,制造胶原及钙化骨基质,其横向分化能力在腹膜钙化、胶原沉积等腹茧症病理改变过程中具重要意义。在AC发病过程中,间皮细胞可能并未消失,而是在外源性刺激因素的作用下发生了转化。
7、其他:胎粪性肠梗阻患者因胎粪致肠穿孔进入腹腔引起无菌性化学性腹膜炎,或肝移植术后轻度腹腔内感染可导致AC。
三、病理组织学
1、肉眼所见:包膜为蚕茧样,壁厚1mm~10mm为一层灰白色、乳白色或淡黄色结缔组织,表面光滑,单腔或多房,可包裹部分小肠或全部小肠,甚至可包裹整个腹腔的脏器。整个肿块能活动,不受壁层腹膜的影响,肿块与腹膜壁层可有疏松的纤维样结缔组织粘连,易于分离。由于小肠被局限包裹,小肠长度往往较正常短,肠系膜亦较短,并可有肠壁增厚、肠腔狭窄和扩张等。
2、光学显微镜下所见:包膜可为正常腹膜样组织,或为增厚的纤维结缔组织。可伴有胶原变化,玻璃样变及慢性炎性反应,非真菌、细菌和寄生虫等微生物感染。

四、临床表现
好发于青少年女性,多数在月经初潮后2年内发病,男性少见。一般无特异性临床表现或仅有轻微的腹部不适、消化不良及腹部肿块等,常于其他疾病手术中或尸检中偶然发现。有临床症状者多以腹部肿块,腹痛,腹胀,恶心,呕吐及肛门停止排气、排便等急性或亚急性肠梗阻症状为主要表现,病情容易反复且病程长短不一,国内报道最长达20余年之久。其临床症状的出现与脏器被纤维膜禁锢形成的腹部包块或机械性肠蠕动是密不可分的。综合文献资料有以下情况时应疑及本病:①青少年患者,尤其是女性月经不调史及不孕史者,出现肠梗阻症状而既往无手术史等明显原因者;②不明原因肠梗阻,既往有反复发作,但可自行缓解者;③常表现为腹痛及恶心呕吐,但缺乏肠梗阻的腹痛、腹胀、恶心呕吐及停止肛门排气排便等四大典型症状者;④腹部触及无压痛、活动性质软的肿块,边界不清,肠鸣音亢进或减弱者,据报道目前占19.3%;⑤既往病史中伴有腹水发生,或长期进行腹膜透析或腹腔化疗者。
五、诊断
由于临床表现缺乏特异性,本病的术前诊断十分困难,诊断率约4.2%。绝大多数病例被误诊为其他疾病,如机械性肠梗阻、慢性阑尾炎等,最终因手术及组织病理学而确诊。除以上临床表现外,以下的一些辅助检查对腹茧症的诊断也有一定帮助。
1、X 线摄片:腹部立位X线平片可表现为肠梗阻,也可为正常或无特异性。胃肠钡餐X线透视可见腹部肿块内为折叠的小肠,肠襻排列成花菜状,加压后肠管不易分离,推动肿块时该段小肠随之移动。X线透视下可见钡剂通过小肠的埋时间明显迟滞,钡柱前进的形状呈“M”形,而正常情况下钡柱经过小肠时呈“Z”形。如果近段小肠扩张或有气液平面说明已有梗阻发生。
2、B型超声:可提示肿物为粘连的肠管,外被有弱回声组织,还可观察到有无腹水及包裹的肠管有无里蠕动。典型的超声特点为肠管被限制在腹后壁,呈强回声团块,疾病后期见膜状物形成。
3、特异性CT征象:①茧样纤维包膜(即“∩”形或类圆形肠管周围等或稍低密度结构)。若纤维膜厚度均匀一致可呈“新月形”,若厚度不一则呈“新月形”或“半圆形”,增强扫描时该膜有延迟强化;②小肠排列呈外缘光整的扭麻花征及盘曲成团的肠管聚集征,肠壁粘连紧密,在矢状位重建时观察更清楚;③肠梗阻征象可在茧状膜包裹前出现,也可在包膜内的小肠出现;④常伴有肠系膜根部团块状影像,并与局部肠管有粘连征象,增强扫描有延迟强化,同时可出现少量腹水,肠系膜血管扩张等间接征象。
4、MRI检查:因其可多方位,多参数成像,能直接显示肥厚、迂曲的肠管、肠管内气体、液体以及大网膜的粘连情况,对本病有较高的诊断价值,为手术前提供更明确的依据。
5、腹腔镜检查:近年来随着腹腔镜的逐渐普及,对腹茧症的可疑病例进行腹腔镜检查可提高诊断率,确诊主要靠术中所见及术后纤维病理组织学检查。
六、鉴别诊断
除与肠梗阻、慢性阑尾炎等相鉴别外,还需与腹膜包裹症(peritoneal encapsulation, PE)鉴别。PE患者小肠被包绕在一层相对正常的腹膜中,其来源是胚胎发育中脐囊残留,属发育异常。与AC不同之处在于PE有小肠外被膜与正常腹膜相似,其内壁与小肠肠管并无黏连,小肠近似位于一个较小的腹膜腔中,肠管蠕动不受限制,肠梗阻的发生率低。
七、治疗
1、非手术治疗:对于临床症状较轻的患者,目前主张采取非手术治疗,包括中医中药治疗、纠正电解质紊乱、胃肠减压等对症治疗;对于无症状,而在检查或手术中发现的患者,可暂不予处理。
2、手术治疗:手术是目前治疗AC的主要方法,对腹胀、腹痛明显或出现肠梗阻症状者均应给予手术治疗。手术原则是彻底切除包膜,松解粘连,切除囊带,解除梗阻。如肠管无病变,尽量避免作肠切除。由于松解粘连过程中容易损伤小肠血管引起肠管血运障碍、或损伤肠壁,引起肠瘘,且有时广泛分离日后可形成广泛粘连,致梗阻发生率增加,所以目前不主张为将包膜彻底切除而过分松解粘连。对于有肠管血运差、肠坏死者可行肠切除吻合术。如术中发现局部小肠粘连成团,且因粘连过重难以分离也可将团块切除,但要注意切除的小肠不宜过长,以免引起短肠综合征及其他并发症。由于部分病例术后仍会形成广泛粘连,故目前多数学者认为在切除纤维膜,松解粘连及缩窄环后应常规行肠排列术,这样即使术后再次梗阻的发生率。但也有部分学者不主张行肠排列术,原因在于如患者术后再次出现肠梗阻,将会大大增加手术难度,也增加肠管损伤和粘连。亦有肠排列术后再次梗阻,手术探查肠粘连严重,不得不切除部分肠管甚至造成肠瘘的报道。目前也有学者主张松解粘连后如无禁忌可附加阑尾切除术。从理论上讲,手术切除阑尾可避免术后发生阑尾炎的危险,以防发作时寻找阑尾困难,更可避免再次手术而引起的腹腔粘连。
术后处理也很重要。由于手术范围广泛,患者术后易出现肠道功能紊乱,部分患者甚至在较长时间内肠道处于麻痹状态,有出现假性肠梗阻的可能,此时应先采取综合的非手术治疗措施,如适当下床活动、应用促进肠蠕动的药物、中医针灸理疗等,耐心观察,切勿急于解除梗阻而再次盲目手术。
综上所述,目前AC仍是一种原因不明、临床少见的腹部疾病。长期以来,临床认识不够,术前诊断困难,漏诊、误诊较多,故藉此文引起临床的注意,以提高对AC的认识。
